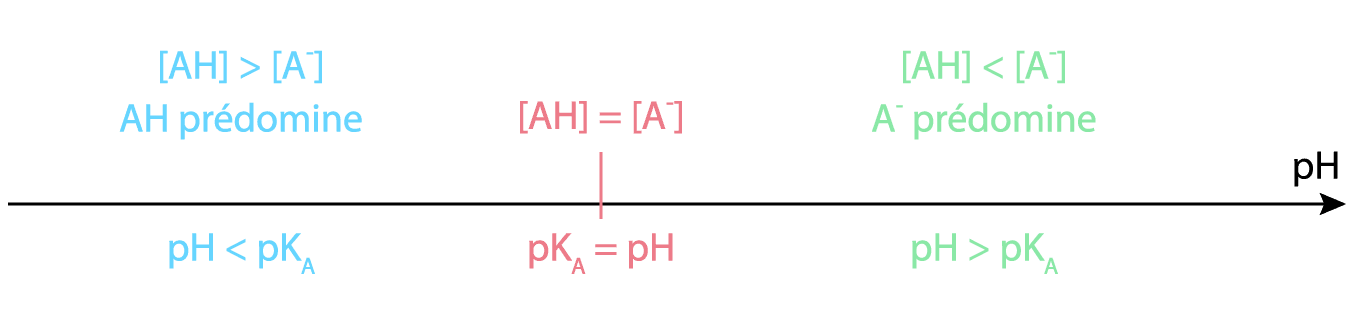Objectif
Comprendre la définition d'un acide et d'une base, reconnaître une réaction acido-basique, et savoir l'écrire et l'équilibrer.

Tableau d’avancement

Méthode tracés des vecteurs vitesse et accélération

Transferts thermiques

Transformations en chimie organique

Formulaire de Physique – Ondes et signaux

Mécanique
Formulaire de Chimie

Fiche outils
UV Visible - IR

Groupes caractéristiques

Mesures et incertitudes

Lunette astonomique - Dipôle RC

Transformations acide-base et pH - Force des acides et des bases 1

Transformations acide-base et pH - Force des acides et des bases 2

Transformations acide-base et pH - Force des acides et des bases 3

Transformations acide-base et pH - Force des acides et des bases 4

Transformations acide-base et pH - Force des acides et des bases 5
Comprendre la définition d'un acide et d'une base, reconnaître une réaction acido-basique, et savoir l'écrire et l'équilibrer.
Comprendre ce qu'est une réaction d'oxydo-réduction, savoir identifier oxydant et réducteur, et équilibrer les équations.

Annales Métropole 2025 — Spé Physique-Chimie sujet 1

Annales Métropole 2025 — Spé Physique-Chimie sujet 2

Annales Métropole 2024 — Spé Physique-Chimie sujet 1

Annales Métropole 2024 — Spé Physique-Chimie sujet 2

Annales Métropole 2023 — Spé Physique-Chimie sujet 1

Annales Métropole 2023 — Spé Physique-Chimie sujet 2

Annales Métropole 2022 — Spé Physique-Chimie sujet 1

Annales Métropole 2022 — Spé Physique-Chimie sujet 2

Annales Polynésie 2021 – Physique-Chimie

Annales Amérique du Nord 2021 — Physique-Chimie
La constante d'équilibre de la réaction d'autoprotolyse de l'eau est appelée produit ionique de l'eau et notée $\rm Ke$.
$\rm \color{green}{H_2O(I)} \color{blue}{~+~} \color{red}{H_2O(I)} \color{blue}{~=~} \color{green}{H_3O^+_{(aq)}} \color{blue}{~+~} \color{red}{HO^-_{(aq)}}$
$\color{red}{\boxed{\begin{array}{ll}\color{black}{\rm Ke = [H_3O^+]_{éq} \times [HO^-]_{éq}}\\
\color{black}{\rm Ke= \color{red}{10^{-14}} \color{black}{\text{ à 25°C}}}\\
\color{black}{\rm \Rightarrow pKe = -\log (Ke) = \color{red}{14}}.\end{array}}}$
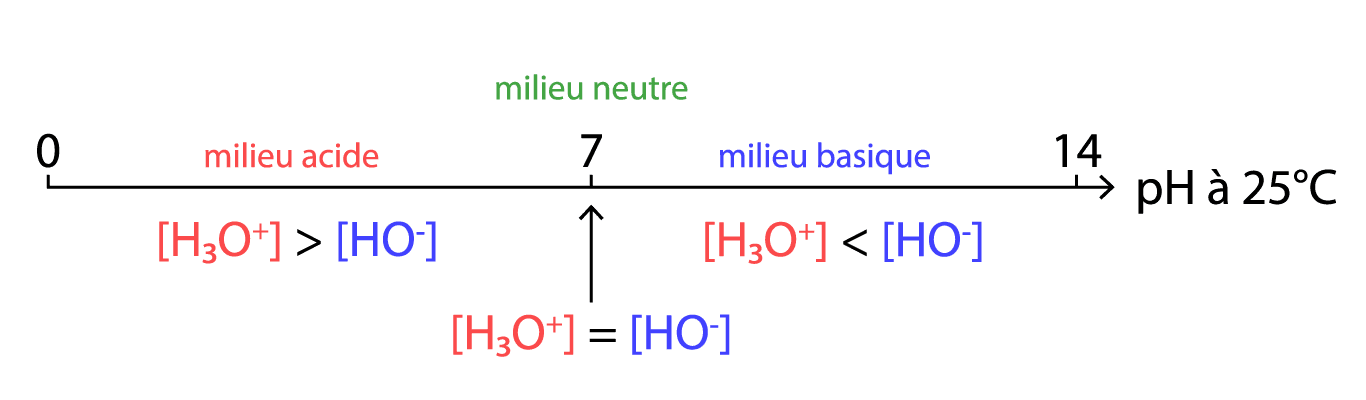
Un acide fort $\rm AH$ réagit totalement avec l'eau. Ces réactions sont caractérisées par une flèche simple entre les réactifs et les produits.
$\rm AH_{(aq)} + H_2O \rightarrow A^-_{(aq)} + H_3O^+_{(aq)}$
Une base forte $\bf A^-$ réagit également totalement avec l'eau.
Calcul du pH :
Un acide faible $\rm AH$ ne réagit pas totalement avec l'eau. Une base faible $\rm A^-$ ne réagit pas totalement avec l'eau non plus.
$\rm AH_{(aq)} + H_2O \leftrightarrows A^-_{(aq)} + H_3O^+_{(aq)}$
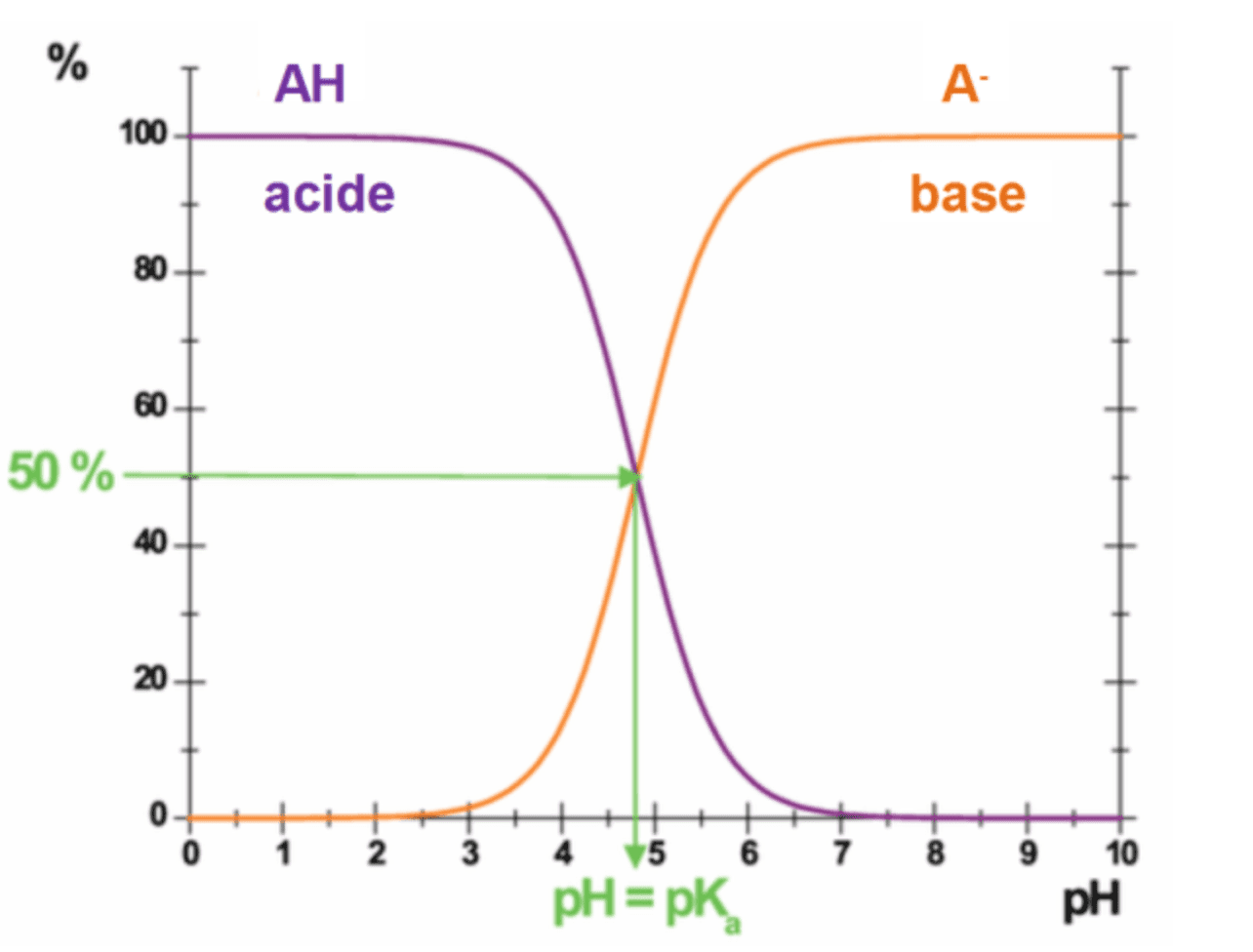
Chaque couple acide faible / base faible est caractérisé par une grandeur sans dimension nommée constante d'acidité, notée $\bf K_A$, du couple $\rm AH / A^-$ :
$\displaystyle \rm K_A = \frac{[H_3O^+]_{eq}\cdot [A^-]_{eq}}{[AH]_{eq}}$ avec $\color{plum}{\boxed{\begin{array}{ll}\color{black}{\text{[Concentration] en } \rm mol.L^{-1}}\\
\color{black}{\rm K_A \text{ sans dimension}}\end{array}}}$
$\rm pK_A = -\log K_A$ et $\rm K_A = 10^{-pK_A}$
Une solution tampon a un pH qui varie peu par addition d'une petite quantité d'acide ou de base, et par dilution modérée.