Structure des entités chimiques organiques
Les alcanes
Les alcanes non cycliques ont pour formule générale $\rm C_nH_{2n+2}$. Le nom des alcanes linéaires prend la terminaison –ane. Un préfixe indique le nombre d'atomes de carbone dans la chaîne carbonée.

Nomenclature des alcanes ramifiés
Pour les alcanes ramifiés : Rechercher la chaîne principale : chaîne carbonée la plus longue. Cette chaîne termine le nom et est nommée comme l'alcane linéaire précédemment. Repérer les ramifications (groupes alkyles) sur cette chaîne. On utilise les mêmes préfixes en fonction du nombre de C de chaque ramification mais avec la terminaison –yl. On numérote la chaîne principale afin que les C portant les ramifications aient les plus petits chiffres possibles. On nomme la molécule en précédant le nom de la chaîne principale par celui des groupes alkyles dans l'ordre alphabétique précédés de leur position sur la chaîne et d'un préfixe multiplicatif (di-, tri-, tétra-) si besoin.

Les alcènes
Les alcènes possèdent une double liaison $\rm C=C$ et leur formule est $\rm C_nH_{2n}$ s'ils sont non cycliques. On remplace –ane par –ène précédé de la position du $\rm C$ de la double liaison et on ajoute $\rm Z$ ou $\rm E$.

Les alcools
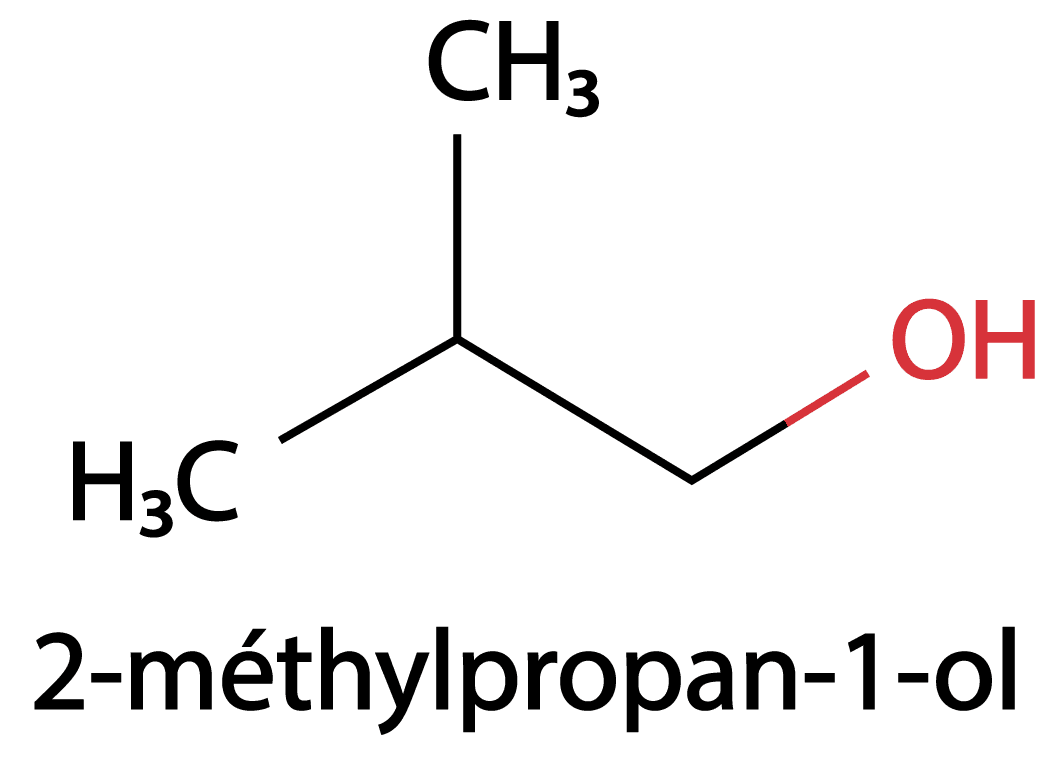
Les alcools sont des molécules comportant le groupe hydroxyle $\rm –OH$. On ajoute –ol à la terminaison –ane précédée de la position du $\rm C$ fonctionnel.
Les composés carbonylés : les aldéhydes et les cétones
Les composés carbonylés possèdent le groupe carbonyle

Chez les aldéhydes, il se trouve en bout de chaîne carbonée, au contraire des cétones. On remplace –ane par –al pour les aldéhydes et par –one pour les cétones précédé de la position du $\rm C$ fonctionnel.

Les acides carboxyliques
Les acides carboxyliques possèdent le groupe carboxyle
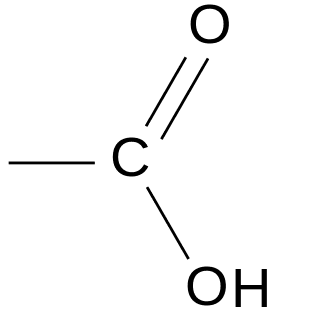
On ajoute –oïque à la terminaison -ane et on précède le nom par le mot acide.

Les esters
Les esters possèdent le groupe ester

Leur nom est en deux parties : la chaîne carbonée contenant le groupe ester prend la terminaison « –oate de » suivi du nom du groupe alkyle lié à l'atome $\rm O$.

Les amines
Les amines possèdent le groupe amino $\rm NH_2$. L'atome $\rm N$ peut être lié à $0$, $1$ ou $2$ $\rm H$. Aux plus simples (contenant $\rm –NH_2$), on ajoute –amine à la terminaison -an précédé de la position la plus petite possible du groupe. Aux autres, on précède le nom par la mention $\rm N-alkyl$ correspondant aux groupes liés à $\rm N$.

Les amides
Les amides possèdent le groupe amide
 .
.
L'atome $\rm N$ est relié à $0,1$ ou $2$ $\rm H$. Le nom des amides les plus simples, contenant $\rm –NH_2$, dérive de celui de l'acide carboxylique, en supprimant « acide » et en remplaçant –oïque par –amide.
Exemplebutanamide

Isomères
Deux molécules sont isomères si elles possèdent la même formule brute mais un arrangement d'atomes différents. Ces molécules isomères n'auront pas les mêmes propriétés physico-chimiques.
On différencie plusieurs types d'isomérie :
Isomères de chaîne
- Les isomères de chaîne ont des chaînes carbonées différentes.
le butane (chaîne linéaire) et le méthylpropane (chaîne ramifiée) ont la même formule brute $\rm C_4H_{10}$.
Le butane : $\scriptstyle \rm CH_3\quad – \quad CH_2 \quad – \quad CH_2 \quad – \quad CH_3$
Le méthylpropane : $\begin{array}{ccc}\scriptstyle \rm CH_3 & \scriptstyle – & \scriptstyle \rm CH & & \scriptstyle – & \scriptstyle\rm CH_3\\ & & | \\& & \scriptstyle\rm CH_3\end{array}$
Isomères de position de fonction
- Les isomères de position de fonction portent le même groupe fonctionnel et ont la même chaîne carbonée mais la fonction n'est pas dans la même position sur la chaîne carbonée.
Le propan-1ol : $\begin{array}{ccc}\scriptstyle \rm CH_2 & \scriptstyle – & \scriptstyle \rm CH_2 & \scriptstyle – & \scriptstyle \rm CH_3\\ | \\ \scriptstyle \rm OH \end{array}$
Le propan-2-ol : $\begin{array}{ccc}\scriptstyle \rm CH_2 & \scriptstyle – & \scriptstyle \rm CH_2 & \scriptstyle – & \scriptstyle \rm CH_3\\ & & | \\ & & \scriptstyle \rm OH \end{array}$
Isomères de fonction
- Les isomères de fonction ne portent pas le même groupe fonctionnel.
Le butanone : $\begin{array}{ccc}\scriptstyle \rm CH_3 & \scriptstyle – & \scriptstyle \rm C & \scriptstyle – & \scriptstyle \rm CH_2 & \scriptstyle \rm CH_3\\ & & \| \\ & & \scriptstyle \rm O \end{array}$
Le butanal : $\scriptstyle \rm CH_3\quad – \quad CH_2 \quad – \quad CH_2 \quad – \quad CH \quad = \quad O$